Serviços Personalizados
Artigo
Indicadores
Links relacionados
 Citado por SciELO
Citado por SciELO
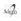 Similares em SciELO
Similares em SciELO
Bookmark
Revista de Actualización Clínica Investiga
versão impressa ISSN 2304-3768
Rev. Act. Clin. Med v.11 La Paz set. 2011
ARTÍCULO
Encefalopatía Uremica
Dra. Cusicanqui G. María Isabel1 Dr. Fernandez C.Juan Carlos2
1 Neurólogo Hospital de Clínicas, Docente Titular Facultad de Odontología UMSA.
2 Neurólogo, Hospital de Clínicas
Resumen
La encefalopatía metabólica se caracteriza habitualmente por antecedente de desorientación y confusión que preceden al inicio del estupor o coma en ausencia de signos motores, frecuentemente existe asterixis, mioclonias, temblor y en los pacientes comatosos la presencia de convulsiones focales o generalizadas aporta datos de disfunción metabólica. La insuficiencia renal aguda o crónica produce encefalopatía urémica. A pesar de extensas investigaciones la causa exacta de la disfunción cerebral en la uremia sigue sin identificarse proponiéndose como agentes causales a la hormona paratiroidea, disbalances en los aminoácidos cerebrales con modificación de los neurotransmisores, y una serie de neurotoxinas tales como la metilguanidina y las moléculas de tamaño medio.
INTRODUCCIÓN
Se utiliza el término encefalopatía metabólica para describir a cualquier proceso que afecte en forma global la actividad cortical a través de la alteración de la función bioquímica del cerebro. Las encefalopatías metabólicas se caracterizan por no presentar anormalidades estructurales primarias. Se debe tener en cuenta, sin embargo, que algunas encefalopatías, tales como la hipóxico-isquémica o la encefalopatía de Wernicke pueden producir daño estructural. Las encefalopatías metabólicas son consecuencia principalmente de desordenes sistémicos y producen una disfunción neurológica global. Habitualmente está afectado el sistema reticular activador ascendente, especialmente en su componente tálamo-cortical.
DEFINICIÓN
La encefalopatía urémica (EU) es un síndrome orgánico cerebral agudo o subagudo que generalmente aparece en los pacientes con insuficiencia renal aguda o crónica cuando la filtración glomerular cae por debajo del 10% de lo normal.
ETIOPATOGENIA
La causa exacta de la encefalopatía urémica(EU) se desconoce. Se han propuesto como agentes causales a los siguientes: trastornos hormonales, estrés oxidativo, acumulación de metabolitos, desequilibrio entre los neurotransmisores de tipo excitatorio e inhibitorio y la alteración del metabolismo intermediario los cuales fueron identificados como factores que contribuyen a la explicación fisiopatológica de la EU.
Recientemente se han sugerido los efectos tóxicos de la hormona paratiroidea (PTH) en el sistema nervioso central (SNC). En la insuficiencia renal aguda y crónica, el nivel de PTH se eleva con elevación concomitante del contenido de calcio de la corteza cerebral. Una combinación de factores, como la hipercalcemia y la disminución del GABA y la actividad de la glicina conducen al balance alterado de los efectos excitatorios e inhibitorios que contribuyen con las alteraciones sistémicas asociadas con la EU. Son varias las sustancias orgánicas que se acumulan, incluyendo la urea, los compuestos de la guanidina, los ácidos úrico e hipúrico, varios aminoácidos, polipéptidos, poliaminas, fenoles y conjugados de fenoles, ácidos fenólico e indólico, acetoína, ácido glucurónico, carnitina, mioinositol, sulfatos, fosfatos y "moléculas medianas." Los niveles de algunos compuestos de guanidina, incluyendo el ácido guanidinosuccínico, la metllguanidina y la creatinina aumentan tanto en los pacientes urémicos no dializados como en los dializados.
En varias regiones del cerebro, los pacientes con falla renal terminal tienen niveles elevados de ácido guanidinosuccínico (>100 veces), metilguanidina (20 veces), guanidina (>100 veces) y creatinina (5 veces). También está comprometida la vía cinurénica, por la cual las moléculas de triptofano se convierte en cinureninas neuroactivas. Otras anormalidades halladas en la encefalopatía uremica son la acidosis, la hiponatremia, la hiperkalemia, la hipocalcemia, la hipermagnesemia, la sobrehidratación y la deshidratación.
Las fases iniciales de la encefalopatía urémica(EU) se caracterizan por la presencia de niveles elevados de glicina, ácidos orgánicos (derivados de la fenilalanina) y triptofano libre, y niveles disminuidos de GABA en el líquido cefalorraquídeo. Se cree que el cerebro urémico utiliza menos ATP y produce menos ADP, AMP y lactato, coincidiendo con una disminución generalizada de la función metabólica.
La transketolasa, hallada principalmente en las neuronas mielinizadas, es una enzima dependiente de la tiamina, en la vía de la pentosa fosfato, que mantiene la vaina de mielina de los axones. Esta enzima es inhibida por el plasma, el líquido cefalorraquídeo, y las fracciones dializadas de bajo peso molecular (<500 Da). La actividad de la transketolasa de los eritrocitos es menor en los pacientes no dializados que en los dializados. El ácido guanidinosuccínico puede inhibir la transketolasa y la transmisión sináptica excitatoria en la región CA1 del hipocampo de la rata, lo cual puede contribuir con los síntomas cognitivos de la EU.
CUADRO CLÍNICO
Los síntomas se inician en forma insidiosa y no se notan a menudo por los pacientes sino por los familiares o cuidadores. En muchos casos el deterioro neurológico proporciona la primera indicación del trastorno metabólico. Los cambios en el sensorio incluyen: letargía, irritabilidad, cambios de personalidad, seguidos por desorientación y confusión. Muchos pacientes están somnolientos pero agitados. Estos síntomas fluctúan, con intervalos de lucidez. El estupor y el coma se hacen evidentes en las formas agudas, y en algunas formas crónicas con severa descompensación. Los hallazgos del examen físico son variables y dependen de la gravedad de la encefalopatía puede mostrar disartria, reflejos primarios y rigidez de nuca. Los reflejos pupilares y los movimientos oculomotores habitualmente son normales. En el 25% de los pacientes presentan signos focales transitorios. Son comunes el temblor, asterixis, y mioclonias multifocales. En los estados avanzados pueden aparecer convulsiones tónico clónicas.
DIAGNOSTICO
El análisis de sangre revela anomalías en los electrolitos y la función renal es anormal. La paratohormona (PTH) y los niveles de calcio son altos.
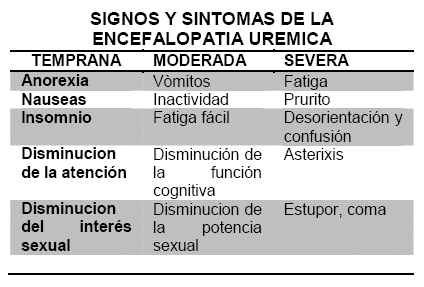
El EEG refleja la severidad de la encefalopatía. Los cambios más comunes son la desaparición de las frecuencias rápidas y la prominencia de las ondas lentas. Es frecuente la presencia de un ritmo theta frontal intermitente, y de actividad paroxística. Las ondas trifásicas, características de la encefalopatía hepática y urémica en sujetos jóvenes, son relativamente raras, y se asocian con deterioro del nivel de conciencia.
La tomografía axial computarizada (TAC) y el estudio del liquido cefalorraquídeo (LCR) ayudan a excluir diagnostico como el hematoma subdural o la infección del sistema nervioso central pero habitualmente sus hallazgos son inespectficos como ser: atrofia cerebral en la TAC o una hiperproteinorraquia en el LCR.
La Resonancia Magnética (RM) puede mostrar un aumento de intensidad de la señal en áreas corticales y subcorticales en los lóbulos parietal y temporal, esto refleja el edema local que se resuelve después de los tratamientos con diálisis.
En varios reportes de casos, se mencionan la presencia de lesiones bilaterales en ganglios básales en pacientes urémicos con diabetes, que se caracteriza por la intensidad de señal alta en T2. Estas lesiones se resolvieron después de la diálisis y se correlacionó con una disminución en el nitrógeno ureico en sangre y los niveles de creatinina. Los potenciales evocados visuales, somatosensoriales y auditivo tiene escaso valor.
TRATAMIENTO
Es importante realizar la corrección del trastorno metabólico, comúnmente mediante la diálisis (hemodiálisis o peritoneal) o el trasplante renal, con los cuales mejora la función renal.
Las convulsiones pueden ser tratadas con fármacos antiepilépticos (FAE) en dosis más bajas que las usuales.
Son de tratamiento de urgencia la presencia de hematoma subdural o la hemorragia intracraneana.
Se debe adecuar las dosis de los medicamentos que el paciente recibe de acuerdo al grado de función renal.
Realizar el tratamiento de la hipertensión arterial sistémica y las infecciones de acuerdo germen identificado o sospecha clínica.
BIBLIOGRAFÍA
1. Young G.: Septic encephalopathy. En Vincent J. (Edit): Yearbook of Intensive Care and Emergency Medicine. Springer, Berlin, 2002. [ Links ]
2. Singh NP, V Sahni, un Wadhwa, S Garg, SK Bajaj, Kohli R. Efecto de la mejora de la anemia en los marcadores eletroneurofisiológica (P300) de la disfunción cognitiva en la enfermedad renal crónica. Int Hemodial. Jul 2006;10(3):267-73 [ Links ]
3. De Deyn PP, D'Hooge R, Van Bogaert PP, Marescau B. Endogenous guanidino compounds as uremic neurotoxins. Kidney Int Suppl. 2001 ;78:S77-83 [ Links ]
4. Vanholder R., de Smet R., Hsu C: Uremic toxicity: the middle molecule hypothesis revisited. Semin Nephrology 14:205-1994 [ Links ]
5. Biasioli S. Neurologic aspects of dialysis. In: Nissenson A, Fine R, eds. Clinical Dialysis. 2005:855-876. [ Links ]
6. Liu M, Liang Y, Chigurupati S, Lathia JD, Pletnikov M, Sun Z, et al. Acute kidney injury leads to inflammation and functional changes in the brain. J Am Soc Nephrol. Jul 2008;19(7):1360-70. [ Links ]
7. Deguchi T, Isozaki K, Yousuke K, Terasaki T, Otagiri M. Involvement of organic anión transporters in the efflux of uremic toxins across the blood-brain barrier. J Neurochem. Feb 2006;96(4):1051-9. [ Links ]
8. Brouns R, De Deyn PP. Neurological complications in renal failure: a review. Clin Neurol Neurosurg. Dec 2004;107(1):1-16. [ Links ]
9. Moe SM, Sprague SM. Uremic encephalopathy. Clin Nephrol. Oct 1994;42(4):251-6. [ Links ]
10. De Deyn PP, Vanholder R, Eloot S, et al. Guanidino compounds as uremic (neuro)toxins. Semin Dial. Jul-Aug 2009;22(4):340-5. [ Links ]
11. Lacerda G, Krummel T, Hirsch E. Neurologic presentations of renal diseases. Neurol Clin. Feb 2010;28(1):45-59. [ Links ]
12. Yoon CH, Seok JI, Lee DK, An GS. Bilateral basal ganglia and unilateral cortical involvement in a diabetic uremic patient. Clin Neurol Neurosurg. Jun 2009;111(5):477-9. [ Links ]
13. Róhl JE, Harms L, Pommer W. Quantitative EEG findings in patients with chronic renal failure. Eur J Med Res. Apr 26 2007;12(4):173-8. [ Links ]
14. Singh NP, Sahni V, Wadhwa A, Garg S, Bajaj SK, Kohli R. Effect of improvement in anemia on electroneurophysiological markers (P300) of cognitive dysfunction in chronic kidney disease. Hemodial Int. Jul2006;10(3):267-73. [ Links ]
15. Jagadha V, Deck JH, Halliday WC, Smyth HS. Wernicke's encephalopathy in patients on peritoneal dialysis or hemodialysis. Ann Neurol. Jan 1987;21(1):78-84. [ Links ]
16. Ropper AH, Brown RH. Uremic encephalopathy. In: Adams and Victor's Principles of Neurology. 8th ed. New York, NY: McGraw-Hill Professional; 2005:969-71 Email: Rev.Med.Act.Clin mail.com Página 568. [ Links ]












